Essai ckinique Alterity
En savoir plus...
Sur le site Clinical Trials (en anglais), retrouvez cet essai :
▪ ATH434
10 à 15 patients AMS concernés et 5 Centres impliqués
Alterity Therapeutics engage son essai clinique en France
C’est un « petit » essai clinique qui commence en France après un début aux Etats-Unis, au Royaume-Uni, en Australie, Nouvelle Zélande, et Italie.
Comme c’est toujours le cas pour les essais de ‘’phase 2’’, il est mené avec un nombre réduit de patients, sélectionnés sur des critères bien définis. Il concernera au niveau mondial une soixantaine de volontaires et, en France, 10 à 15 personnes souffrant d’AMS suivies dans l’un des 5 Centres de référence ou de compétences ci-dessous :
- Bordeaux
- Toulouse
- Lille
- Marseille
- Paris La Pitié-Salpêtrière
Chacun de ces Centres commence donc la sélection, parmi les personnes qu’il suit, des 2 ou 3 candidats qui devraient être inclus dans l’essai d’ici fin septembre.
Les patients retenus devront avoir moins de 75 ans, être concernés depuis moins de 4 ans par les premiers signes moteurs de l’AMS (lenteur, tremblements, raideur, troubles d’équilibre…), être capables de marcher au moins 10 mètres sans aide (canne autorisée) et chuter moins d’une fois par semaine.
L’essai d’ATH 434 va durer 54 semaines. Les patients prendront pendant 52 semaines, par voie orale, ou bien une dose A, ou bien une dose B, ou bien un placebo. Cet essai est mené en « double aveugle » : ni le malade, ni le neurologue investigateur ne sait ce que le tirage au sort a réservé au le patient.
Il a pour objectifs de déterminer la plus petite dose efficace et la posologie optimale du candidat-médicament qui pourra être testé plus largement en phase 3, mais aussi à identifier les éventuels effets indésirables. Onze visites en présentiel et 6 consultations à distance sont prévues pendant la durée de l’essai.
Cibler l’excès de fer dans le cerveau
Le métabolisme du fer dans le cerveau est complexe. Ce fer cérébral est nécessaire. Il joue un rôle important dans la production de dopamine. Il contribue aussi à la production par les 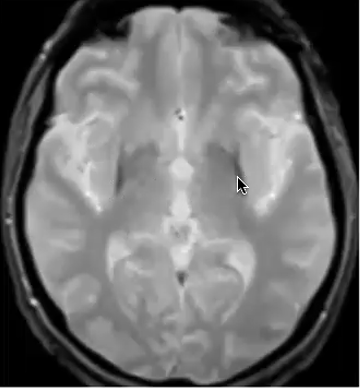 cellules gliales de l’indispensable myéline qui gaine les neurones comme un isolant. Mais s’il est présent en trop grande quantité, il interagit négativement avec l’alpha-synucléine et peut favoriser son mauvais repliement et la formation d’agrégats toxiques.
cellules gliales de l’indispensable myéline qui gaine les neurones comme un isolant. Mais s’il est présent en trop grande quantité, il interagit négativement avec l’alpha-synucléine et peut favoriser son mauvais repliement et la formation d’agrégats toxiques.
ATH434, le candidat-médicament d’Alterity Therapeutics est une ‘’petite molécule’’ qui passe facilement la barrière hémato-méningée et s’associe avec le fer cérébral. Au terme des 12 mois de l’essai clinique, l’évolution des niveaux de fer cérébral et d'α-synucléine agrégée sera mesurée chez les patients qui participent au test.
Deux traces sombres apparaissent à l’IRM, l’une est fléchée, à droite.Elles signalent une accumulation anormale de fer dans le putamen, une partie du cerveau impliquée dans la réalisation de mouvements volontaires. Cette accumulation est un facteur des symptômes comme la lenteur, la raideur et les tremblements. Son repérage à l’IRM est l’un des signes qui conduisent au diagnostic d’AMS.
Glossaire
Cellules gliales
Ce sont les cellules qui forment l’environnement des neurones. Elles jouent un rôle de soutien et de protection du tissu. Elles entourent les neurones et participent au contrôle de l'en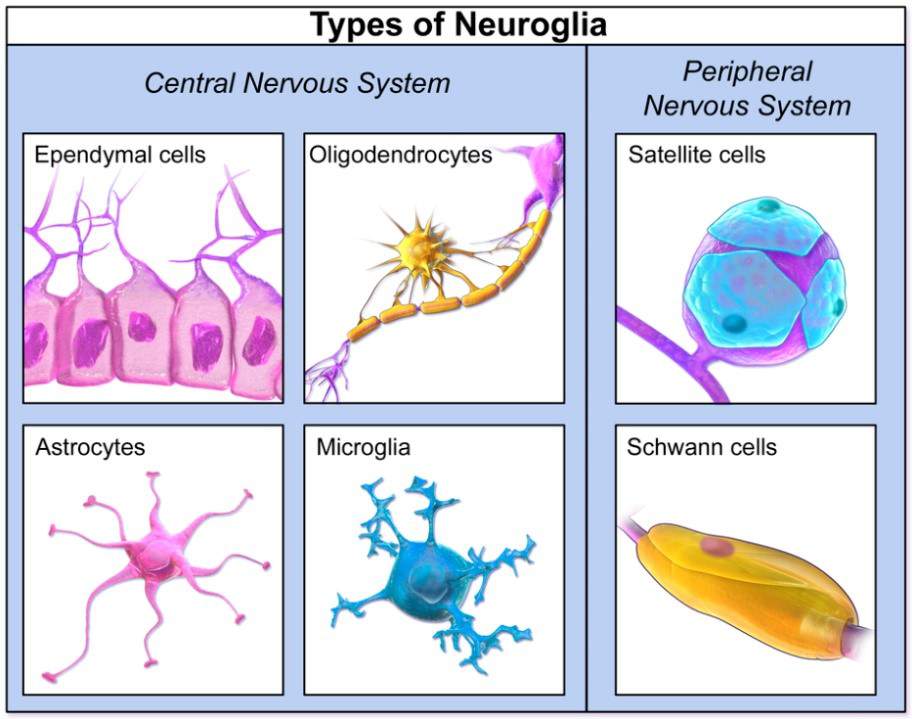 vironnement chimique et électrique en leur fournissant des nutriments, de l’oxygène et en éliminant leurs déchets. Ces cellules produisent par exemple la myéline, une substance qui sert d'isolant aux fibres nerveuses.
vironnement chimique et électrique en leur fournissant des nutriments, de l’oxygène et en éliminant leurs déchets. Ces cellules produisent par exemple la myéline, une substance qui sert d'isolant aux fibres nerveuses.
Il y aurait, dans notre système nerveux, à peu près autant de cellules gliales que de neurones, soit environ 100 milliards. Les cellules gliales sont différentes au sein du système nerveux central et du système nerveux périphérique, elles n’ont pas non plus la même origine dans leur développement.
● Les cellules gliales du système nerveux central (SNC) qui dérivent des glioblastes du tube neuronal embryonnaire, sont de 3 types :
- les astrocytes qui assurent un lien fonctionnel entre vaisseaux et neurones, apportant substrats énergétiques aux neurones et les débarrassant des produits de dégradation ;
- les oligodendrocytes à l’origine de la gaine de myéline des neurones ;
- les épendymocytes qui forment les parois qui délimitent les différentes cavités du SNC et sont responsables de la synthèse du liquide céphalo-rachidien (LCR)
● Les cellules gliales du système nerveux périphérique (SNP), dérivent des crêtes neurales embryonnaires. Ce sont les cellules satellites avec une fonction analogue à celle des astrocytes et les cellules de Schwann qui forment chacune la gaine d’un seul neurone, à la différence des oligodendrocytes qui « s’occupent » chacun d’une dizaine de neurones.
Dopamine
La dopamine est l'une des nombreuses substances chimiques qui servent de neurotransmetteurs dans le cerveau. La noradrénaline, l'adrénaline, la sérotonine et l'acétylcholine sont d'autres neurotransmetteurs. On a pu établir une relation entre le déficit en un neurotransmetteur spécifique et des troubles nerveux comme la maladie de Parkinson. La L-dopa (levodopa), prescrite dans le traitement de la maladie de Parkinson, est un précurseur direct de la dopamine qui passe la barrière hémato-encéphalique et peut être transformée en dopamine dans le cerveau.
80% des neurones 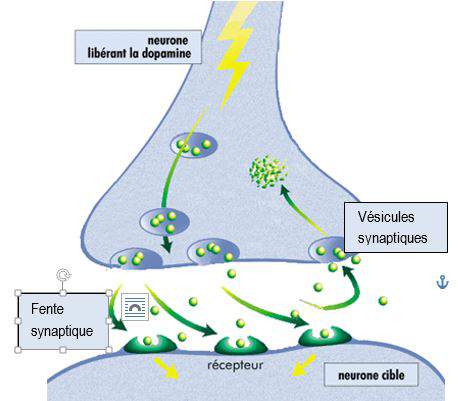 dopaminergiques contenus dans le cerveau sont situés dans la substance noire.
dopaminergiques contenus dans le cerveau sont situés dans la substance noire.
Synthétisée dans les terminaisons pré-synaptiques des neurones dopaminergiques, la dopamine est chargée dans des vésicules synaptiques qui la libèrent dans la fente synaptique à l’arrivée d’un potentiel d’action.
La dopamine libérée dans la fente est en partie captée par des récepteurs se trouvant sur la cellule postsynaptique et transmet ainsi le signal neuronal. Environ 80 % de la dopamine libérée est recaptée par les neurones dopaminergiques présynaptiques par des transporteurs sélectifs DAT (dopamine active transporter), qui contrôlent ainsi de façon précise la concentration dopaminergique, à la fois dans le temps et dans l’espace.
Voir aussi :
- voies dopaminergiques
- neurotransmetteur
- synapse
